作者:沈淑華/有勁基因
有勁部落格文章《簡述實務上判斷游離 DNA品質好壞的依據》中曾提到:臨床上可透過「液態活檢」,也就是利用偵測血液中的「生物標記」(biomarker)來進行癌症診斷,達到癌症精準醫學預測和預防的目標。近年來已有不少研究採用癌症患者液態活組織內的血液標記做為觀察對象,例如血液循環腫瘤DNA(ctDNA)與游離DNA(cfDNA)。本篇文章要介紹的是另一種生物標記─腫瘤突變負荷量(tumor mutation burden; TMB)。
黑色素瘤是第一個利用免疫檢查點抑制劑治療成功的惡性腫瘤,然而這類治療方法在4到5成患者的身上卻無法達到效果,甚至對6成患者還會造成嚴重的副作用;像這種時候,如果有能提供效果鑑別預測的生物標記可用,就能提前預測治療的效果了。腫瘤突變負荷量,就是一種可以預測免疫療法效果的生物標記。
本篇要介紹的研究,該團隊從35位接受ipilimumab(抗CTLA-4)和nivolumab(抗PD-1)治療的黑色素瘤病患血液中採集了循環腫瘤DNA與游離DNA,進行一連串試驗;並藉由生物資訊運算,將腫瘤突變負荷量標準化後劃分為以下三級:
低腫瘤突變負荷:腫瘤突變負荷量小於3.3 Mut/Mb
中腫瘤突變負荷:腫瘤突變負荷量介於3.3到23.1 Mut/Mb之間
高腫瘤突變負荷:腫瘤突變負荷量大於23.1 Mut/Mb
然後針對「中/低腫瘤突變負荷(負荷量≦ 23.1 Mut/Mb)」和「高腫瘤突變負荷(負荷量>23.1 Mut/Mb)」兩類別去探討腫瘤突變負荷量與整體存活率(overall survival; OS;指經過一段追蹤觀察的時間後,觀察整組病人存活的比率)之間的關係。
由下圖一可看出,只要偵測到循環腫瘤DNA、或偵測到循環腫瘤DNA/游離DNA任一有升高的情形,患者的存活率就會降低。作者為了瞭解腫瘤突變負荷量的高低是否會影響上述結果,又做了進一步分析。結果發現,中/低腫瘤突變負荷患者只要被偵測出循環腫瘤DNA(無論循環腫瘤DNA的量有沒有升高)、或是偵測到游離DNA量有升高情況,患者的存活率都不佳(如圖二所示)。
圖一、腫瘤突變負荷量與黑色素瘤存活率之間的關係
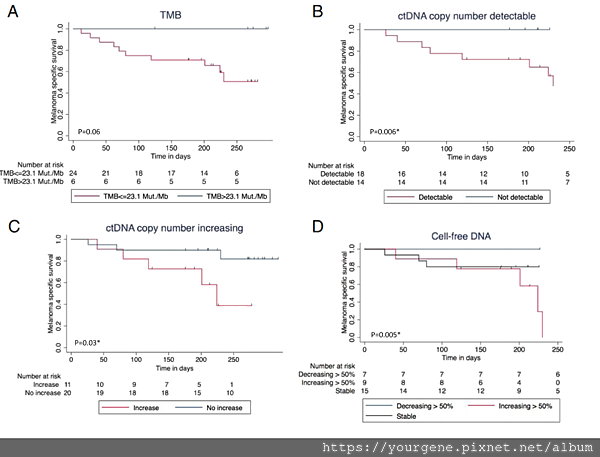
如圖A所示,腫瘤突變負荷量(TMB)大於23.1 Mut/Mb的患者(黑色線條標示),其存活率(縱軸)比腫瘤突變負荷量≦23.1 Mut/Mb(紅色線條標示)來得高。實驗過程中,只要有偵測到循環腫瘤DNA(圖B紅色線條)、或者偵測到循環腫瘤DNA有拷貝數明顯升高的情形(圖C紅色線條)、或是偵測到游離DNA量升高超過50%(圖D紅色線條),這些患者的存活率都明顯較低。(圖片出處: Forschner A., et al. Journal for ImmunoTherapy of Cancer. 2019 Jul;7:180-194)
圖二、腫瘤突變負荷量高低與血液循環腫瘤DNA/游離DNA之間的關係
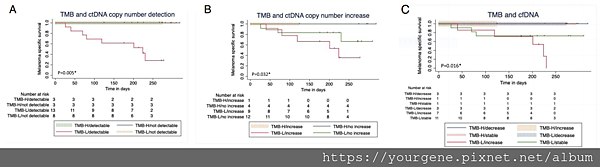
被偵測到循環腫瘤DNA的中/低腫瘤突變負荷患者(TMB-L),其存活率明顯較低;高腫瘤突變負荷(TMB-H)患者則不受循環腫瘤DNA影響(圖A)。中/低腫瘤突變負荷患者,不論循環腫瘤DNA有拷貝數是否有升高,存活率都不佳(圖B)。中/低腫瘤突變負荷患者如果游離DNA量有升高情況,存活率都不佳(圖C)。(圖片出處: Forschner A., et al. Journal for ImmunoTherapy of Cancer. 2019 Jul;7:180-194)
綜合以上結果可得知,腫瘤突變負荷量的高低確實會左右整體存活率。如何將本文報導的這項技術應用於臨床並實際提升治療效果,將會是一大挑戰。
參考文獻
1. Forschner A., et al. Tumor mutation burden and circulating tumor DNA in combined CTLA-4 and PD-1 antibody therapy in metastatic melanoma - results of a prospective biomarker study. Journal for ImmunoTherapy of Cancer. 2019 Jul;7:180-194. Retrieved from https://doi: 10.1186/s40425-019-0659-0.





 留言列表
留言列表 {{ article.title }}
{{ article.title }}
