作者:伊喬伶/有勁基因 (有勁基因講座報導系列─游舒涵醫師講座)
案例(二)多次侏儒症胎兒的懷胎病史
產前分子檢測的發展從早期大片段染色體異常的觀測,到DNA微陣列晶片技術的發展(DNA microarray),再進展到全基因體定序(WGS; Whole Genome Sequencing)及全外顯子定序(WES; Whole Exome Sequencing),每個階段都各有優缺點。然而,相較於目前其他的分子檢測,全基因體定序及全外顯子定序能針對特定案例,更完整地偵測出胎兒的染色體變異。有勁基因股份有限公司(Yourgene Health (Taiwan) Co., Ltd.)在2019年台灣醫療科技展期間,邀請了林口長庚醫院婦產部游舒涵醫師分享該院婦產部醫師團隊們運用全外顯子定序技術於產前臨床檢測的經驗。
醫師簡介
游舒涵醫師畢業於長庚大學醫學系,獲有英國胎兒醫學基金會(FMF)第一孕期篩檢認證,現任財團法人長庚紀念醫院林口分院婦產部研究醫師;在產檢及接生之餘,也會投入產科醫學論文的撰寫並參與學會活動。展會中游醫師分享了兩起病人案例,第一個案例是「近親生育與胎兒生長結構異常」的產後胎兒致病研究,第二個案例是將孕婦「數次侏儒症胎兒的懷孕病史」與定序結果運用在之後的產前檢測。
摘要─多次侏儒症胎兒的懷胎病史
從案例一可以得知,將全外顯子定序應用在胎兒疾病檢測時,除了需要對胎兒本身進行檢測之外,也建議雙親一同進行全外顯子定序檢測,以便由家庭定序結果獲得更多線索。下面要分享的是利用一家三口全外顯子定序(Trio Whole Exome Sequencing)協助醫師們找出胎兒致病的主要關鍵的案例。
門診診斷
本案例中的24歲懷孕媽媽,本身未患有疾病,近期也沒有服用藥物,育有一位健康的女兒(第二胎);但她連同這次,共有兩次侏儒症胎兒的懷胎病史(第一胎及第三胎),皆於懷孕中後期時終止妊娠,理由是在產前超音波檢查時發現胎兒的長骨未照週數成長。本次懷孕是她的第三胎,因發現胎兒異常而在第三孕期來到林口長庚醫院希望終止妊娠。醫師與家屬討論後,基於孕婦懷胎史中曾有數胎出現重複的長骨異常發育徵狀,建議需進一步了解是否有基因變異而導致侏儒症(Dwarfism)發生的情況。
一般在進行產前超音波檢查時,醫師會評估胎兒的頭、肚子及腿長;而本案例的這個胎兒的頭圍及腹圍與該週數的胎兒標準差異不大,但腿的股骨長以及其他長骨的發育卻落後了4~6週,有可能是罹患了骨骼發育異常症(Skeletal Dysplasia),又稱侏儒症(Dwarfism),此病會導致骨骼形成及生長不良。侏儒症種類目前已鑑定出450多種,其中少數種類甚至會造成死胎。本起案例的胎兒所罹患的侏儒症類型為低磷酸酯酶症 (hypophosphatasia, HPP)。
檢測過程及基因變異簡介
這位媽媽在終止妊娠後,針對父母及本案例這第三胎被終止妊娠的胎兒做了全外顯子定序檢測,找出了ALPL這個標的基因,再針對這個基因,為父母、正常女兒以及死胎進行桑格定序(Sanger Sequencing)確認。結果發現,本案例被終止妊娠的第三胎、正常女兒與媽媽在Chr1的21880591(hg19)位置皆帶有同樣的單套缺失變異(heterozygous deletion)基因,而父親的基因在這個位置的序列則是正常的。根據台灣人體生物資料庫(Taiwan Biobank)的數據,在台灣這個基因發生缺失變異(deletion)的機率約為十萬分之一。遺憾的是,爸爸的這個基因在另外兩個位置:21894597(hg19)與21894598(hg19)剛好也有變異,變異型態為單套插入變異(heterozygous insertion)所導致的框移突變(frameshift);在台灣這個基因發生單套插入變異的機率也是十萬分之一,而這第三胎竟剛好又遺傳到來自父親的變異,由於胎兒兩條染色體的ALPL基因同時從父母雙方都遺傳到變異,因而致病。正常女兒並未從父方遺傳到變異,除了來自母方的21880591(hg19)位點變異外,其餘基因序列皆正常,因此女兒和母親皆為單一帶因者。下方表一列出這對父母及第三胎經全外顯子定序檢測後所獲得的基因變異狀況。
表一、家庭ALPL基因變異的帶有狀況

圖片來源:游舒涵醫師/林口長庚婦產部
根據圖二家庭基因譜系的解釋,爸爸的ALPL基因有兩個位置發生了單套插入的基因變異,而媽媽有一個位置發生單套缺失的基因變異;第一胎及第三胎有可能因為從父母雙方都遺傳到變異的ALPL基因,因而罹患了侏儒症(由於第一胎並非在長庚醫院執行終止妊娠,因此未經實驗確認,僅根據臨床診斷推斷)。而被終止妊娠的第三胎,根據全外顯子定序以及桑格定序也證實該基因的確有基因複合雜合體突變(Compound heterozygous mutation)的情況發生。不幸的是,該位母親後來又意外懷有第四胎,於林口長庚進行羊膜穿刺,再次利用桑格定序進行檢測,胎兒同樣又被確診罹患跟第三胎一樣的低磷酸酯酶症。總結,這個家庭的父母親在ALPL基因上各帶有不同位置的變異,若其子女從父母親雙方都遺傳到發生變異的ALPL基因,就會引發疾病。
圖二、家庭的基因譜系
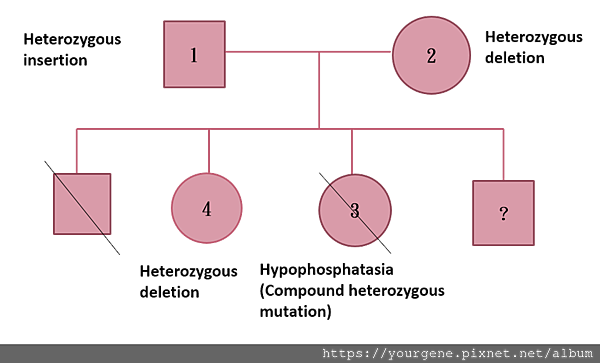
圖片來源:游舒涵醫師/林口長庚婦產部
低磷酸酯酶症是常染色體隠性遺傳骨骼發育異常疾病,為侏儒症的一種。該病症形成的原因包括隱性基因變異(homozygous mutation)、或是ALPL基因上發生了複合雜合體突變。其典型的病徵為長骨較扁較短、胸廓狹小等。全外顯子定序技術幫本案例的家庭找出不斷遇到這種妊娠狀況的原因。該母親先後總共終止妊娠三次,對於母體來說是非常大的傷害及負擔;未來若想要再次懷孕生產,院方也有提供這對父母後續的相關諮詢,例如可以考慮試管嬰兒搭配植入前胚胎診斷等等,而在胚胎植入前,需先確認這個胚胎未帶有雙方的變異,如此就可望避免再發生前述終止妊娠的情況。
結論
目前次世代定序的方案有數種,其中全外顯子定序與全基因體定序在臨床上經常作為醫師輔助診斷的工具。這兩種定序主要的差異在於前者僅定序分析人類的外顯子區域,因此與後者比起來,耗費的時間與金錢都較少。定序完畢後,我們還需要去了解哪些基因變異的位點是具有意義的,因此進行分析比對所採用的資料庫也是非常重要的關鍵。醫師取得NGS最後檢測結果之後,臨床上還會再利用桑格定序進行重複確認,以確保分析結果的準確性。
全外顯子定序檢測結果與定序的深度、樣本前處理及針對外顯子區域的捕捉(capture)效率有密切的關係,因此在臨床上想要廣泛使用全外顯子定序去尋找與疾病有關的DNA變異,實際上還有些瓶頸存在。2016年在Nature發表的一篇研究1,運用全外顯子定序技術對六萬多人的基因進行了分析,發現人類基因變異出現在外顯子上的比例比我們原本預期的更高,約每8個鹼基(bases)中就有一個會發生變異,不過這些變異點位還需要更深入去做分析,才能確定其變異是否足以致病。
全外顯子定序目前學術界一般認為對神經科特別能提供幫助,尤其是小兒神經科2,3。許多神經發展遲緩的小朋友,臨床上經常得不到確切的病因診斷。而在全外顯子定序檢測後,約四成都可取得病因診斷3。這樣的確診結果,對家屬、照顧者的心理多少都有一定的緩和作用,同時也能幫助希望生育下一胎的家屬提前做準備。有一篇研究發表在2019年的Lancet論文,其內容主要是分析有哪些跟胎兒發育結構異常(fetal anomaly)有關的病因診斷可以透過全外顯子定序來輔助診斷5。該篇論文主要的研究對象為產前超音波檢查結果異常的胎兒,病因診斷比例最高的是「骨骼發育異常(skeletal anomalies)」,如同上述分享的兩個案例;此外,就是心血管疾病(Cardiac)、脊髓相關疾症(Spinal)與腦相關疾病(Brain)...等等的4。然而,並非所有臨床案例都能找到病因,例如大動脈轉位或心臟異常,這些案例或許可找出基因變異的點位,但比對疾病資料庫及分析之後,卻依然無法找出致病主因。
American College of Medical Genetics and Genomics (ACMG)的報告指出,目前胎兒的全外顯子定序檢測仍不能算是常規的醫療項目5,臨床醫療工作人員必須先對病人的疾病與狀況是否適合進行全外顯子定序檢測進行評估。院方為家屬提供諮詢時,必須給家屬專業的解釋及介紹,主要是因為並非每位受檢者在全外顯子定序檢測後都能找到變異的基因點位;即便找得到點位,也未必可以解釋變異基因對臨床上病情影響的嚴重程度。例如同時有兩位小孩帶有同位點的變異,他們在臨床上病情表現的嚴重程度有可能會不同,所以在基因診斷以及諮詢上讓家屬充分理解是非常重要的。
基因定序檢測目前並無法取代婦產科臨床上主要的診斷工具。受檢胎兒的染色體若有非整倍數變異或是拷貝數變異,單純從基因序列突變的角度上去進行檢視,結果會是正常的,換句話說,這種情況下,全外顯子定序也無法發揮功用。產檢時建議要依照狀況去選擇適當的診斷工具,才能有效發揮檢測或診斷的意義及必要性。
參考文獻
1. Lek, M. et al. Analysis of protein-coding genetic variation in 60,706 humans. Nature. 2016 Aug; 536(7616):285-291. Retrieved from https://www.nature.com/articles/nature19057
2. Srivastava, S. et al. Meta-analysis and multidisciplinary consensus statement: exome sequencing is a first-tier clinical diagnostic test for individuals with neurodevelopmental disorders. Genetics in Medicine. 2019 Nov ; 21(11):2413-2421. Retrieved from https://www.nature.com/articles/s41436-019-0554-6
3. Kuperberg, M. et al. Utility of Whole Exome Sequencing for Genetic Diagnosis of Previously Undiagnosed Pediatric Neurology Patients. Journal of Child Neurology. 2016 Aug; 31(14):1534-1539. Retrieved from https://doi.org/10.1177/0883073816664836
4. Lord, J. et al. Prenatal exome sequencing analysis in fetal structural anomalies detected by ultrasonography (PAGE): a cohort study. Lancet. 2019 Feb; 393(10173):747-757. Retrieved from https://doi.org/10.1016/S0140-6736(18)31940-8
5. Robert, C. et al. ACMG recommendations for reporting of incidental findings in clinical exome and genome sequencing. Genetics in Medicine. 2013 June; 15:565-574. Retrieved from https://www.nature.com/articles/gim201373





 留言列表
留言列表 {{ article.title }}
{{ article.title }}
