作者:林佑軒/有勁基因
循環腫瘤DNA(circulating tumor DNA; ctDNA)是腫瘤組織釋放到血液中的短片段DNA,雖然其確切的生成代謝機制至今仍然不明,但ctDNA的存在可以提供許多和腫瘤相關的訊息,且不需透過侵入性採檢,就能幫助及早發現腫瘤,或者在治療後協助腫瘤復發的監控。ctDNA目前可以提供的訊息究竟有哪些?從下圖一就能一見端倪。
圖一、ctDNA可提供的訊息
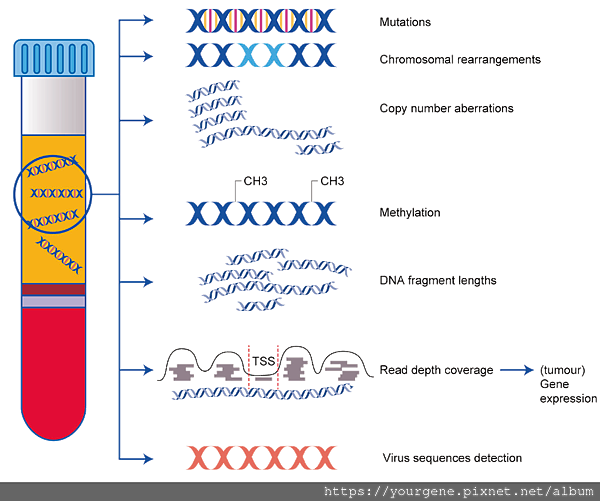
從血漿ctDNA的分析結果,我們能找出腫瘤相關突變、染色體倍數異常與染色體重組的現象。此外,源自不同組織的細胞擁有自己特有的甲基化型態,透過ctDNA甲基化分析,能推測腫瘤所在的組織;而利用ctDNA長度較一般游離DNA短的特性,可以進行長度篩選提升ctDNA的含量比例。另外,用次世代定序去分析轉錄起始點(transcription starting sites; TSS)上的定序深度,可以藉此推測基因的表現量;與病毒感染有關的特定癌症,也能藉由分析游離DNA是否含有病毒序列,提前預知罹癌的風險。(圖片來源: Keller, L., et al., Br J Cancer. 2021 Jan;124:345-358)
一、基因突變 (mutations)
偵測血液循環DNA(circulating cell-free DNA; cfDNA)是否含有腫瘤相關的基因突變,能幫助提早發現腫瘤的存在;而透過分析cfDNA 中ctDNA的基因變異,則可幫助了解腫瘤的特性與預後狀況。此外在選擇治療用藥時,亦可依照基因變異的種類,選擇合適的藥物或治療策略。不過就如有勁部落格《循環腫瘤DNA檢測的瓶頸》一文所提,許多透過cfDNA所偵測到的基因突變其實是源自白血球而非腫瘤,該如何降低檢測結果的偽陽性率仍是目前的一大挑戰。
二、染色體倍數與DNA結構性異常
腫瘤的基因體經常呈現染色體倍數異常(copy number aberrations)或DNA結構性異常(例如: 倒置(inversions)、轉位(translocations)、插入(insertions)與刪除(deletions))等現象,這些特性 ctDNA也有,因此偵測cfDNA中是否有染色體倍數與DNA結構性異常,也是癌症初期篩檢腫瘤的一種方式。然而據研究指出1,ctDNA含量至少要在5%以上才有可能測出染色體倍數與DNA結構性的異常,而 ctDNA在cfDNA中所佔的比例有可能很低,尤其在腫瘤初期ctDNA實際含量比例甚至可能低於5%,所以檢測結果有偽陰性的疑慮。除此之外,由於未罹癌的人也有出現染色體倍數與DNA結構性異常的可能,所以想確定從cfDNA發現的異常究竟是不是從腫瘤來的,也是相當大的挑戰。
三、DNA片段化的型態(DNA fragmentation patterns)
我們在《去蕪存菁:長度篩選對ctDNA偵測的效益》一文曾提到ctDNA片段長度較其他cfDNA來的短,所以可以透過長度篩選去提高ctDNA的比例,進而提升各種檢測的正確性。除了DNA片段的長度,DNA片段化的型態也能用來推測重要腫瘤基因的表現量。如下圖二所示,用次世代定序(Next generation sequencing; NGS)去分析轉錄起始點(transcription starting sites; TSS)附近的cfDNA定序量,可以進一步推論出染色質(chromatin)的多寡。被定序到的cfDNA片段含量若較少,代表chromatin也較少,較有利轉錄的進行,該基因的表現可能較高。只不過,要想從cfDNA去分析某腫瘤的ctDNA特定基因表現量,該ctDNA在cfDNA的含量比例必須至少佔75%,才能正確進行評估2;但在自然情況下,ctDNA比例幾乎不可能達到這個程度,除非有特殊技術能精準且大幅地提升ctDNA比例,不然,要想實際執行這個應用其實是相當困難的。
圖二、從DNA 片段化的型態去推測基因表現量
A
B
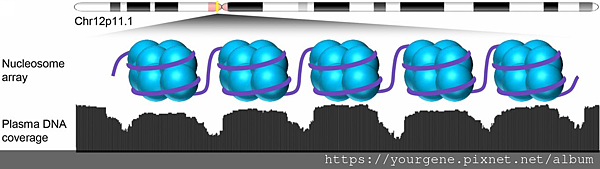
圖二、 (A)用NGS去定序cfDNA, chromatin部分(水藍色)的定序深度(coverage)較深,代表被定序到的cfDNA片段主要是原本是包覆在組織蛋白(histone)上的DNA。(圖片來源3: Sun, K., et al., Proc Natl Acad Sci U S A. 2018 May;115(22):E5106-E5114)
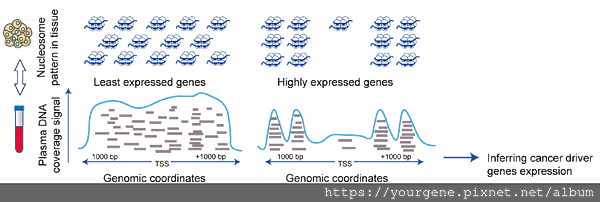
(B)將NGS定序出的序列與參考基因體(reference genome)進行比對,分析轉錄起始點(TSS)附近的定序深度。右圖的TSS區域定序深度較低,表示chromatin分佈少,有利於轉錄的進行,所以能判斷該基因可能是高度表現的基因。左圖在TSS區域有定序到cfDNA片段,表示chromatin分佈多,不利於轉錄的進行,所以判斷該基因可能是低度表現的基因。(圖片來源4: Keller, L., et al., Br J Cancer. 2021 Jan;124:345-358)
四、DNA 甲基化(DNA methylation)
DNA甲基化是表觀遺傳編碼(Epigenetic code)的一部分,透過DNA甲基化位置的不同,可以讓相同基因體的細胞表現出不同的功能。不同組織、不同功能的細胞都各有其獨特的甲基化型態;研究指出5,甲基化型態相當穩定,細胞即便發生病變,例如癌化,也不容易改變其甲基化的型態。若將cfDNA的甲基化型態拿來比對人體各個組織的甲基化特有型態,可以分析出個別cfDNA片段的來源組織;利用這個特性,便能從找到的ctDNA去推測腫瘤可能存在於身體的哪個組織或器官6。不過要解開cfDNA的甲基化型態,其實驗費用高昂,且需要較長的時間去進行樣品處理及資料分析,想實際普及應用到臨床上,目前可能還是有困難。
五、病毒的DNA片段
有些癌症與病毒的感染有關,例如鼻咽癌與人類皰疹病毒第四型(Epstein-Barr virus; EBV)。在受到這些病毒感染後,人類cfDNA中也會測到這些病毒的DNA片段;因此分析cfDNA是否含有特定容易致癌病毒的DNA片段,也能提早提供醫師與病患警示。雖然感染這些病毒不代表絕對會罹癌,但這些資訊會是後續健康檢查頻率與策略的重要參考。有勁基因與香港Take2合作的Prophecy™檢測便是本於這個基礎而進行鼻咽癌的篩查。
分析ctDNA的確能提供我們許多的資訊,從中也能衍伸出許多的檢測應用,有機會讓病人透過抽血去提早發現腫瘤,甚至知道腫瘤的特性及後續用藥策略。不過這些資訊衍伸出的應用目前仍有不少侷限,例如高偽陽或偽陰性的問題。若想再提升結果的正確性,除了不斷進行技術改良,也需要更透徹地去研究與了解ctDNA的生成代謝途徑與特性並整合ctDNA的各種資訊。相信未來ctDNA的檢測應能像非侵入性產前篩檢那樣普及於一般民眾,在腫瘤初期提供具高度正確性的檢測方式。
參考文獻
1. Chan, K.C.A., et al. Cancer genome scanning in plasma: detection of tumor-associated copy number aberrations, single-nucleotide variants, and tumoral heterogeneity by massively parallel sequencing. Clin. Chem. 2013 Jan;59(1):211-224. Retrieved from https://doi.org/10.1373/clinchem.2012.196014
2. Ulz, P., et al. Inferring expressed genes by whole-genome sequencing of plasma DNA. Nat. Genet. 2016 Oct;48(10):1273-1278. Retrieved from https://doi.org/10.1038/ng.3648
3. Sun, K., et al. Size-tagged preferred ends in maternal plasma DNA shed light on the production mechanism and show utility in noninvasive prenatal testing. Proc Natl Acad Sci USA. 2018 May;115(22):E5106-E5114. Retrieved from https://doi.org/10.1073/pnas.1804134115
4. Keller, L., Belloum, Y., Wikman, H., and Pantel, K. Clinical relevance of blood-based ctDNA analysis: mutation detection and beyond. Br J Cancer. 2021 Jan;124:345-358. Retrieved from https://doi.org/10.1038/s41416-020-01047-5
5. Epigenomics, R., et al. Integrative analysis of 111 reference human epigenomes. Nature. 2015 Feb;518(7539):317-330. Retrieved from https://doi.org/10.1038/nature14248
6. Sun, K., et al. Plasma DNA tissue mapping by genome-wide methylation sequencing for noninvasive prenatal, cancer, and transplantation assessments. Proc. Natl Acad. Sci. USA 2015 Oct;112(40):E5503-5512. Retrieved from https://doi.org/10.1073/pnas.1508736112





 留言列表
留言列表 {{ article.title }}
{{ article.title }}
